本文來自《中國器審》��,我特別認同文中作者觀點——以臨床價值為導(dǎo)向開展醫(yī)療器械研制���,臨床應(yīng)用價值應(yīng)是醫(yī)療器械研制的起點��,亦是醫(yī)療器械研制的終點��,從臨床應(yīng)用開始��,最后回歸到臨床應(yīng)用��。對于我國醫(yī)療器械行業(yè)來說����,這幾年逐步由仿制到自研的過渡��,越來越多器械創(chuàng)新工作者�����,器械創(chuàng)新企業(yè)走在創(chuàng)新�����、創(chuàng)業(yè)、創(chuàng)造這條路上����,因此,轉(zhuǎn)載此文章供大家閱讀���,并作為商業(yè)用途����。
引言:本文來自《中國器審》�,我特別認同文中作者觀點——以臨床價值為導(dǎo)向開展醫(yī)療器械研制,臨床應(yīng)用價值應(yīng)是醫(yī)療器械研制的起點���,亦是醫(yī)療器械研制的終點,從臨床應(yīng)用開始��,最后回歸到臨床應(yīng)用��。對于我國醫(yī)療器械行業(yè)來說��,這幾年逐步由仿制到自研的過渡�����,越來越多器械創(chuàng)新工作者,器械創(chuàng)新企業(yè)走在創(chuàng)新��、創(chuàng)業(yè)����、創(chuàng)造這條路上,因此����,轉(zhuǎn)載此文章供大家閱讀��,并作為商業(yè)用途�����。
引言
金屬骨針作為骨科手術(shù)中的關(guān)鍵植入器械之一,廣泛應(yīng)用于骨折固定����、畸形矯正及關(guān)節(jié)融合等領(lǐng)域。近年來�����,隨著材料科學(xué)和制造技術(shù)的進步�����,產(chǎn)業(yè)涌現(xiàn)出越來越多全新設(shè)計產(chǎn)品,金屬骨針的設(shè)計逐漸從單一功能向精準化��、個性化方向發(fā)展�����。為更好地保證產(chǎn)品臨床使用的安全有效性����,這類產(chǎn)品的上市前非臨床研究尤顯重要。本文從臨床價值導(dǎo)向出發(fā)����,探討金屬骨針產(chǎn)品的設(shè)計開發(fā)、風險管理及技術(shù)審評的關(guān)鍵點����。
一��、以臨床價值為導(dǎo)向設(shè)計金屬骨針產(chǎn)品的必要性
1.臨床需求的驅(qū)動
骨科醫(yī)療器械市場雖然技術(shù)迭代迅速��,但臨床效果并未同步提升�。研究表明���,約20%的骨科植入物因設(shè)計不合理導(dǎo)致術(shù)后并發(fā)癥,如假體松動�����、感染和力學(xué)失效等[1]�,而傳統(tǒng)醫(yī)療器械的設(shè)計存在過度關(guān)注技術(shù)參數(shù)而忽視臨床實際,導(dǎo)致部分植入物與患者解剖結(jié)構(gòu)匹配度不足����,術(shù)后并發(fā)癥發(fā)生率居高不下。有文獻顯示�����,傳統(tǒng)骨針在骨質(zhì)疏松患者中易發(fā)生松動或斷裂�����,導(dǎo)致二次手術(shù)率高達15%[2]�����。這種脫節(jié)現(xiàn)象凸顯了以臨床價值為導(dǎo)向的設(shè)計必要性。臨床價值導(dǎo)向要求設(shè)計需直接回應(yīng)未被滿足的需求�,如縮短手術(shù)時間、降低感染風險等�。
2.政策法規(guī)的推動
各國監(jiān)管機構(gòu)正逐步加強對醫(yī)療器械臨床價值的重視。例如����,我國國家藥品監(jiān)督管理局在發(fā)布的《醫(yī)療器械臨床評價技術(shù)指導(dǎo)原則》[3]中強調(diào)真實世界數(shù)據(jù)的重要性。美國FDA在2017年發(fā)布的《突破性醫(yī)療器械計劃》[4]也明確要求以臨床終末效益為核心評價指標�����。醫(yī)療器械服務(wù)于臨床實踐�����,高水平的設(shè)計開發(fā)才能更好地實現(xiàn)產(chǎn)品的高質(zhì)量發(fā)展��,從而滿足人民日益增長的美好健康需要���。
3.醫(yī)療經(jīng)濟學(xué)的考量
以臨床價值為導(dǎo)向的設(shè)計不僅能提高治療效果���,還能降低醫(yī)療成本。研究表明�,通過優(yōu)化醫(yī)療器械產(chǎn)品設(shè)計可減少術(shù)后并發(fā)癥,可使單例患者的綜合治療成本降低30%[5]����。
4.患者個體化差異的考量
骨科醫(yī)療器械設(shè)計需從解剖、生物力學(xué)和手術(shù)操作三個維度解構(gòu)臨床需求�,不同解剖部位(如股骨與指骨)對骨針的力學(xué)性能要求差異顯著。因此��,醫(yī)療器械的設(shè)計需基于大數(shù)據(jù)分析或影像學(xué)建模�����,實現(xiàn)解剖適配性��。
二����、金屬骨針類產(chǎn)品設(shè)計開發(fā)的關(guān)注點
金屬骨針類產(chǎn)品作為骨科比較成熟的醫(yī)療器械產(chǎn)品之一,其生產(chǎn)研發(fā)歷史相對較長���。此類器械的設(shè)計開發(fā)需緊密圍繞骨針類產(chǎn)品在臨床的預(yù)期適用范圍��,如四肢骨折復(fù)位時部分植入人體做牽引�����、配合外固定支架進行四肢骨折固定或單獨植入等�����,因此�,金屬骨針的設(shè)計開發(fā)需重點關(guān)注以下幾點:
1.材料選擇與性能優(yōu)化
材料類型:如316L不銹鋼(成本相對低)、鈦合金(生物相容性較優(yōu))���、鈷鉻合金(耐磨性較強)的取舍需權(quán)衡力學(xué)性能與生物學(xué)響應(yīng)[6]�。
表面改性:如羥基磷灰石(HA)涂層可提升骨整合��,但需控制結(jié)晶度(60%-70%)以避免剝落風險[7]����。
2.結(jié)構(gòu)設(shè)計與制造工藝
幾何參數(shù):如螺紋深度、螺距需匹配骨密度分布����。有限元分析(FEA)顯示,錐形設(shè)計可減少應(yīng)力集中達40%[8]��。
制造技術(shù):如增材制造(如SLM)支持復(fù)雜結(jié)構(gòu)�,但需驗證內(nèi)部缺陷率(應(yīng)<0.1%)[9]。
3.生物相容性與力學(xué)驗證
參照GB/T 16886.1進行生物學(xué)評價����,必要時開展相應(yīng)生物學(xué)試驗����,如細胞毒性����、致敏性及植入后局部反應(yīng)���。
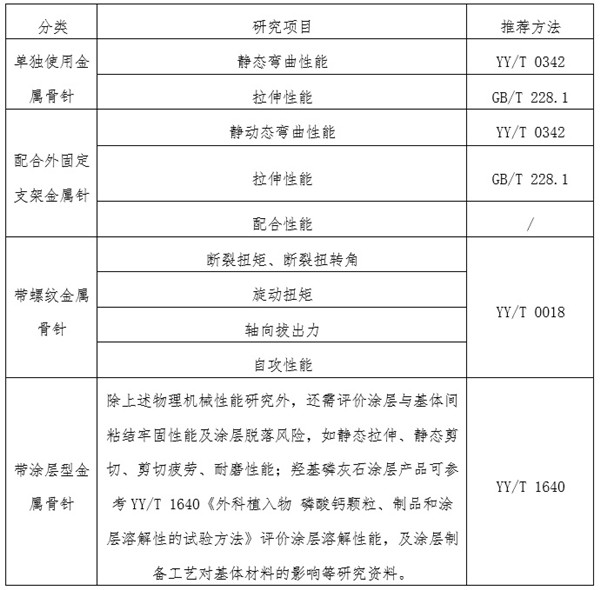
力學(xué)測試:可參考相應(yīng)標準要求����,對骨針開展動靜態(tài)力學(xué)性能測試����,詳見表1。
三��、金屬骨針類產(chǎn)品技術(shù)審評的關(guān)注點
為指導(dǎo)注冊申請人對金屬骨針注冊申報資料的準備及撰寫���,同時也為技術(shù)審評部門對金屬骨針類產(chǎn)品注冊申報資料的審評提供參考�����,我們在現(xiàn)行法規(guī)和標準體系以及當前認知水平下總結(jié)了此類產(chǎn)品在技術(shù)審評時需關(guān)注以下內(nèi)容:
1.非臨床研究部分
產(chǎn)品風險管理資料
醫(yī)療器械安全和性能基本原則清單
產(chǎn)品技術(shù)要求與性能指標����,如抗拉強度、斷裂伸長率�、不銹鋼產(chǎn)品的耐腐蝕性能、表面缺陷����、表面粗糙度,外觀�、關(guān)鍵尺寸及公差 、無菌��、環(huán)氧乙烷殘留量�����;對于帶涂層骨針���,還需明確涂層表面粗糙度����、涂層與基體粘接強度�����。
研究資料:產(chǎn)品物理性能研究(見表1),化學(xué)/材料表征研究����、生物學(xué)特性研究、穩(wěn)定性研究���。
表1金屬骨針物理和機械性能研究及推薦方法
2.臨床評價部分
對于已納入《免于臨床評價醫(yī)療器械目錄》的傳統(tǒng)金屬骨針需按照《列入免于進行臨床評價醫(yī)療器械目錄產(chǎn)品對比說明技術(shù)指導(dǎo)原則》開展評價,但對于目錄外金屬骨針產(chǎn)品還需開展更為詳細的臨床評價��,如增加超出范圍產(chǎn)品的臨床評價資料���,同時建議重視真實世界證據(jù)�����,盡可能多的收集相應(yīng)真實世界的臨床使用數(shù)據(jù)[10]���,重視不良反應(yīng)事件報告。
結(jié)語
綜上����,如何實現(xiàn)以臨床價值為導(dǎo)向的金屬骨針產(chǎn)品設(shè)計開發(fā)����,首先要求從事醫(yī)療器械生產(chǎn)��、設(shè)計開發(fā)的企業(yè)需要非常熟悉國家現(xiàn)行的醫(yī)療器械生產(chǎn)�����、經(jīng)營�����、注冊等相關(guān)法律法規(guī)及指導(dǎo)文件�,認真學(xué)習(xí)各類文件,正確運用指導(dǎo)文件����,關(guān)注金屬骨針類產(chǎn)品在臨床使用中的痛點,堅持以臨床價值為核心�,重視風險管理,嚴格落實產(chǎn)品質(zhì)量可靠���,體系穩(wěn)定的要求���,進一步完善上市后的追蹤反饋��。未來�����,隨著精準醫(yī)療與智能制造的融合��,相信會有更多以臨床需求為價值導(dǎo)向的骨針產(chǎn)品上市�����,進一步改善患者預(yù)后����,這需要我們的審評體系同步革新以平衡創(chuàng)新與風險管理�����。
如有醫(yī)療器械注冊咨詢服務(wù)需求��,歡迎您隨時方便與杭州證標客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò)���,聯(lián)系人:呂工,電話:18058734169,微信同���。